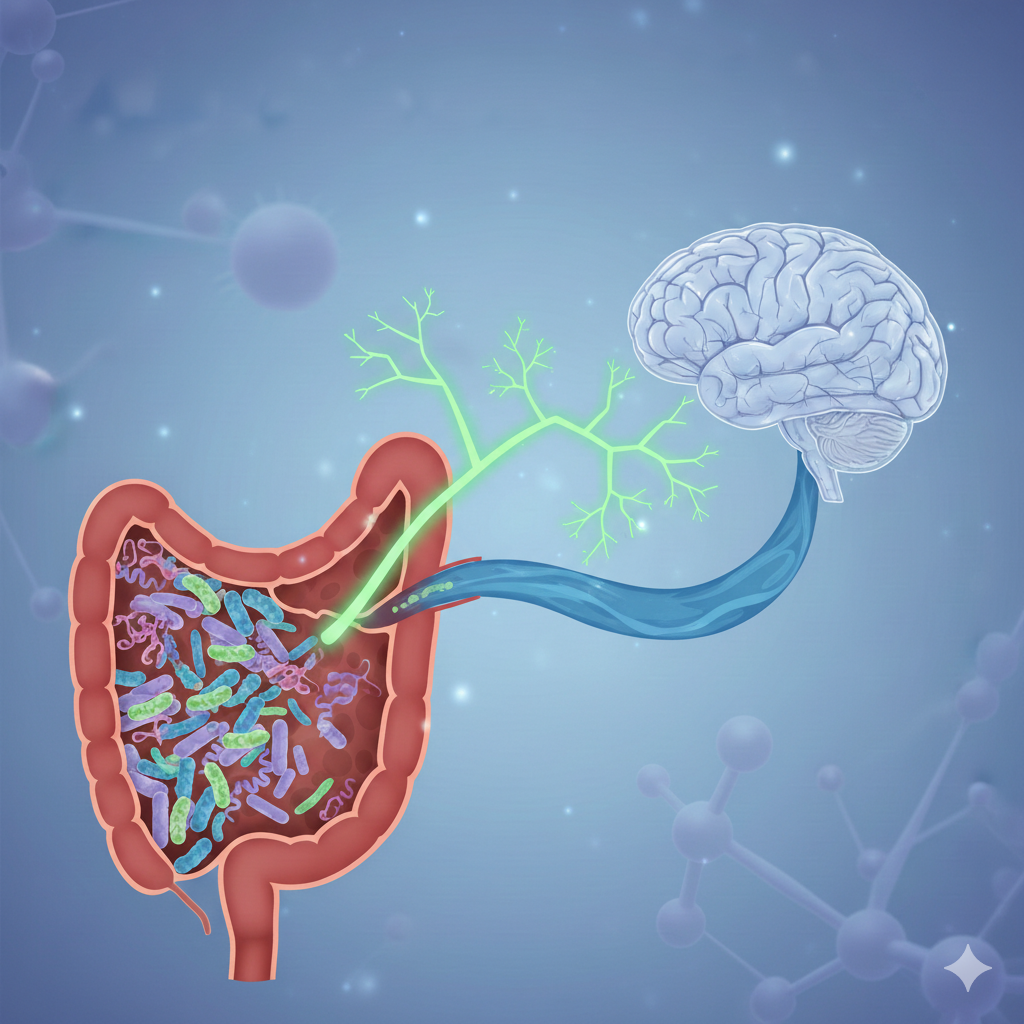
Microbiota y Neuroinflamación
Los científicos definen la microbiota como “el conjunto de los microorganismos (todas las bacterias, arqueas, protozoos, helmintos y virus) presentes en un entorno. La mayor población de microorganismos en el cuerpo humano reside en el intestino, se trata de la “microbiota intestinal”.
¿Qué relación tiene precisamente esta sobre la salud de nuestro sistema nervioso, y cómo influye en la neuroinflamación?.
¿Qué es la neuroinflamación?
Es la respuesta inflamatoria en el cerebro y se caracteriza por la activación de la microglía y la producción en el cerebro de mediadores pro-inflamatorios. Las células endoteliales vasculares, junto con los astrocitos, son los componentes mayoritarios en la barrera hematoencefálica (BHE).
Las células endoteliales liberan diferentes mediadores pro-inflamatorios en el cerebro cuando están estimuladas por una inflamación sistémica como la producida en el intestino.
Además, las células de la microglía (los macrófagos del cerebro) pueden ser activados por estos mediadores pro-inflamatorios, liberando varios tipos de quimiocinas con propiedades inflamatorias.
Estos mecanismos contribuyen al desarrollo de la neuroinflamación en el cerebro.
¿Cómo podemos saber si existe neuroinflamación?
Algunos de los síntomas más frecuentes son:
• Nebulosa mental (Brain fog).
• Estado de ánimo bajo, apatía.
• Irritabilidad, ansiedad.
• Dificultad para concentrarse y pérdida de memoria.
• Somnolencia, lentitud de pensamiento.
Además, sabemos que la neuroinflamación juega un papel importante en la patogénesis de diferentes patologías del SNC como son el autismo, la Esclerosis múltiple, el Parkinson, el Alzheimer o la misma depresión o ansiedad.
¿Qué provoca la neuroinflamación?
Cualquier situación que pueda provocar una inflamación sistémica de manera mantenida, va a ser un factor de riesgo para acabar provocando una situación de inflamación en nuestro cerebro. Factores como:
• Disbiosis y permeabilidad intestinal.
• Permeabilidad de la barrera hematoencefálica.
• Una alimentación inflamatoria, basada en productos y no en alimentos de calidad.
• Estrés crónico, el llamado “distres”.
• La falta de Descanso.
• El sedentarismo
• Tóxicos como determinados medicamentos, el alcohol o el tabaco
• La endotoxemia como la producido en caso de permeabilidad intestinal, sobrecrecimiento bacteriano o fúngico, infecciones por parásitos..o incluso el mismo estreñimiento.
DEL BRAIN-GUT-AXIS AL MICROBIOMA-BRAIN-GUT-AXIS
Hace tiempo que sabemos que existe una comunicación entre el intestino y el cerebro, y que esta es bidireccional, influyendo uno sobre el otro de manera constante. Es el famoso “gut-brain-axis”.
Ahora bien, en los últimos años ha entrado en esta ecuación un tercer factor, la microbiota. Esta, va a influir en este proceso de comunicación por diferentes vías:
• En estudios realizados se ha encontrado que la colonización bacteriana promueve la función de la barrera intestinal y la “educación” del sistema inmune. Las interacciones con las bacterias son probablemente el factor más potente que conduce a la maduración normal del sistema inmune. La colonización intestinal aberrante en la vida temprana se ha asociado con un mayor riesgo de enfermedades no transmisibles en la edad adulta.
• Por su comunicación directa con el sistema inmunitario, generando que este libere citoquinas inflamatorias o antiinflamatorias en función del estado de la misma. Por ejemplo, en un Sibo, la señalización será claramente de activación de la inmunidad innata, generando un estado inflamatorio por una sobreactivación de TLR4.
• Mediante la fabricación de metabolitos como derivados del metabolismo del triptófano, los cuales mejoran la función de los astrocitos en el sistema nervioso central, influyendo en la integridad de la barrera hematoencefálica.
• Mediante la fabricación de AGCC (butirato, propionato, acetato) que influirán en la respuesta inflamatoria intestinal y también en la activación de la microglía en el sistema nervioso.
• Fabricando neurotransmisores presentes todos ellos en la respuesta neurológica cerebral (serotonina, GABA, Dopamina, acetilcolina, etc.)
Así que como vemos, la microbiota influirá en nuestro sistema nervioso central y por consiguiente en nuestra conducta y estado de ánimo.
Barrera hematoencefálica
La barrera intestinal (con sus enterocitos, mucina, IgAs, péptidos antimicrobianos etc..) presenta una permeabilidad selectiva. Quiere decir esto, que permitirá el paso de ciertas sustancias como nutrientes o electrolitos, pero en cambio nos protegerá de la entrada a nuestro organismo de microorganismos, macromoléculas y tóxicos entre otros. Esto también pasa en nuestro sistema nervioso central.
El cerebro, con sus múltiples funciones vitales, está protegido de sustancias
potencialmente dañinas en el torrente sanguíneo por una estructura en forma de valla llamada “barrera hematoencefálica (BHE)”.
La BHE, es un entramado de células unidas entre sí por “tight juctions” (uniones estrechas) que mantienen fuera la mayoría de las sustancias y permiten que unas pocas entren en el cerebro. Al hablar de sustancias dañinas nos referimos a metales pesados, pesticidas, PCB, microorganismos y algunos péptidos, mientras que permite el paso de oxígeno, hormonas, nutrientes y células del sistema inmunitario que informen al cerebro de cómo están las cosas en la periferia.
Leaky gut, leaky brain
Existe evidencia que cuando tenemos un intestino permeable tenemos muchos números de sufrir un exceso de permeabilidad en la BHE. ¿Cómo? se va a producir la activación del inflamasoma en el intestino, generando una cascada de citoquinas inflamatorias que llegaran a la BHE.
Además habrá una traslocación de moléculas de ciertas bacterias (LPS), tóxicos de las mismas, y antígenos alimentarios que también van a llegar a la BHE. Todo esto va a generar una señal de alarma a nuestro SNC, generando neuroinflamación. Si esta situación es mantenida puede afectar las uniones estrechas y va a provocar permabilidad de la BHE o “leaky Brain”.
La BHE se vuelve más permeable dejando pasar sustancias nocivas, aumentando la neuroinflamación. Tener en cuenta que un cerebro pinchado es un cerebro inflamado. Así que vemos como una disbiosis intestinal, mediante la permeabilidad intestinal, puede acabar generando permeabilidad de la barrera hematoencefálica y con ello neuroinflamación (mediada por la activación del sistema inmunitario dentro del cerebro).
Esta situación si es mantenida va a generar un ambiente inflamatorio con una alta carga oxidativa, contexto perfecto para que, si existe la susceptibilidad genética, se desarrolle una patología neurodegenerativa.
Los estudios están revelando cómo las variaciones en la composición de la microbiota intestinal influyen en todos los aspectos de la fisiología, incluida la función cerebral e incluso el comportamiento.
En términos de neurociencia y enfermedad psiquiátrica, el campo aún está en su infancia, pero se acumula evidencia de que tiene un papel clave.
Es por ello que decimos que una disbiosis intestinal, está implicada en la patogenia de estas enfermedades. Algunos ejemplos de esta relación:
• En la enfermedad de Alzheimer la permeabilidad intestinal y la disrupción de la BBB van a facilitar que sangre periférica con beta amiloide y citosinas inflamatorias ingresen al cerebro y exprese la patología en neuronas vulnerables.
• En la enfermedad de parkinson evidencias emergentes parecen indicar la acumulación de alfa-sinucleina en el S.N.Entérico antes que en el S.N.Central.
• Tener exceso de bacterias intestinales del género Clostridium (sobretodo perfingers y Difficile) y Pseudomonas facilita sufrir neuroinflamación, ya que producen p-cresol. Una sustancia que actúa como una neurotoxina, y se ha asociado a alteraciones del SNC (autismo, TDA, incluso esquizofrenia).
PSICOBIÓTICO
El concepto de psicobiótico es el de una bacteria viva que, cuando se ingiere en cantidades adecuadas, confiere beneficios para la salud mental.
En este sentido podemos hacer dos intervenciones:
• Asegurar la ingesta/administración de prebióticos como (FOS) y (GOS), ya que mejoran la diversidad de la microbiota intestinal. Estos prebióticos son fermentados en el colon, liberando acetato, propionato, butirato y otros SCFAs.
De ellos, el butirato es capaz de atravesar la barrera hematoencefálica, ejerciendo efectos neuroprotectores y antidepresivos.
• Administrar cepas de bacterias específicas en función de los efectos que queramos obtener. Por ejemplo, algunas familias de Lactobacillus y Bifidobacterium, son capaces de secretar el neurotransmisor GABA (ansiolítico natural), o la E.Coli Nissae 1917 y los Enterococcus producen 5 hidroxitriptófano, precursor de la famosa serotonina, o la familia de los Bacillus producen dopamina.
Estos neurotransmisores producidos en la periferia influyen de manera indirecta en nuestro cerebro ya que no pueden cruzar la barrera hematoencefálica, por lo que su acción es principalmente local a nivel intestinal. Recordemos que la comunicación entre el intestino y el cerebro tiene diferentes rutas: nervio Vago, por las citoquinas del sistema inmunitario que informaran del estado inflamatorio o de inmunotolerancia que hay a nivel intestinal, y por estos neurotransmisores y diferentes proteínas sintetizadas en él.
Microbiota intestinal y sistema inmunitario
Nuestra microbiota intestinal, que es el ecosistema constituido por microorganismos presentes en nuestro intestino, es un componente clave en nuestro sistema inmunológico. El tejido linfoide asociado al intestino (GALT, por sus siglas en inglés) constituye la parte más compleja y extensa de nuestro sistema inmunitario, cuya acción defensiva es bastante potente. Además, en el intestino encontramos la mayor cantidad de células de nuestro organismo encargadas de producir anticuerpos. Los anticuerpos son proteínas utilizadas por el sistema inmune para identificar y neutralizar los elementos patógenos que llegan a nuestro organismo.
Las enfermedades asociadas a una respuesta anormal de nuestro sistema inmunitario han aumentado de forma significativa en los últimos 50 años. Parece ser que una de las principales causas subyacentes de este aumento de prevalencia reside en nuestra microbiota intestinal. Nuestra comunidad microbiana intestinal se encuentra compuesta por bacterias que conviven de manera simbiótica, bien sea en relación de comensalismo o de mutualismo. Además, en este ecosistema también encontramos bacterias y otros microorganismos con potencial patógeno. En el caso de una microbiota normal o saludable, toda esta población microbiana se encuentra en un correcto equilibro, de forma que todos conviven en consonancia y realizando correctamente sus funciones. No obstante, este complejo equilibrio puede romperse, algo que es relativamente sencillo con el estilo de vida y alimentación actual, lo que da lugar a una microbiota alterada, que recibe el nombre de disbiosis.
Qué es la disbiosis intestinal y tipos
La disbiosis intestinal, explicada de una forma sencilla y general, es una alteración en la estructura de la comunidad microbiana intestinal, que resulta anormal frente a lo que consideramos una microbiota sana y diversa.
Encontramos tres tipos de disbiosis intestinal:
1-Disbiosis intestinal por una mayor presencia de bacterias patógenas
En nuestra microbiota también residen microorganismos con potencial patógeno, pero cuando nuestra microbiota se encuentra en un correcto equilibrio los microorganismos patógenos se mantienen bajo control, sin causar ningún problema. Sin embargo, bajo determinadas circunstancias, se puede producir un sobrecrecimiento de estas bacterias patógenas (conocidas en inglés como pathobionts), siendo aquí cuando empiezan a surgir los problemas. En concreto, lo que ocurre es que se produce una expansión de las proteobacterias, en particular las de la familia Enterobacteriaceae, entre las que se encuentra la tan conocida E.coli y la Shigella, entre otros. En pruebas realizadas en ratones, se ha comprobado que aquéllos que padecían colitis y enfermedad de Crohn tenían una microbiota en la que existía esta mayor presencia de bacterias patógenas, algo que nos muestra la relación existente entre el desarrollo de las enfermedades autoinmunes y el estado de nuestra comunidad microbiana intestinal.
2-Disbiosis intestinal por pérdida de microorganismos beneficiosos
Las bacterias beneficiosas que alberga nuestra microbiota cumplen funciones muy relevantes, entre las que se encuentra la producción de ácidos grasos de cadena corta (SCFAs), como el butirato. Estos ácidos grasos ejercen una acción antinflamatoria y se estudian por su posible potencial en la prevención e incluso tratamiento de diversas enfermedades crónicas. Los ácidos grasos de cadena corta producidos por nuestras bacterias beneficiosas intestinales suprimen la inflamación mediante la reducción de la migración y proliferación de las células inmunes, reducen también diferentes tipos de citoquinas y además, actúan induciendo la apoptosis.
Nuestras bacterias intestinales beneficiosas, entre las que se encuentran las Bifidobacterias y los Lactobacillus, cumplen, además, otras muchas funciones aparte de la producción de ácidos grasos de cadena corta. Tener una adecuada presencia de Bifidobacterias en nuestra microbiota influye positivamente en nuestro sistema inmunológico y además, actúan combatiendo la inflamación y protegen nuestra barrera intestinal.
Sabiendo el efecto positivo que ejercen los microorganismos beneficiosos intestinales sobre nuestra salud, podemos entonces entender por qué su pérdida puede afectarnos de forma negativa. Esta pérdida de microorganismos beneficiosos intestinales que nos conduce a una disbiosis intestinal, en la actualidad se encuentra principalmente provocada por los hábitos de vida y alimentación, los cuáles describiremos más adelante.
3-Disbiosis intestinal por pérdida de diversidad microbiana
Cuanto mayor sea la diversidad de microrganismos que resida en nuestra microbiota, mejor se encontrará ésta, al igual que nuestra salud en general. El conjunto de estudios realizados al respecto vienen a concluir que una mayor diversidad microbiana intestinal se traduce en más beneficios para el huésped (nosotros). De hecho, se ha demostrado que los niños con menor diversidad microbiana intestinal presentan una mayor susceptibilidad a sufrir alergias y asma.
¿Cómo afecta a nuestra salud la disbiosis intestinal?
Tener alterada la microbiota intestinal supone un problema para nuestra salud, ya que nuestro sistema inmune se encontrará más débil, nuestra barrera intestinal se encontrará menos protegida y además, produciremos menos ácidos grasos de cadena corta (los cuales, tal y como he mencionado anteriormente, parecen jugar un papel bastante interesante en la prevención de diversas patologías crónicas, especialmente el cáncer colorrectal, el síndrome metabólico y además, debido a su acción antiinflamatoria, parecen ejercer una acción beneficiosa en casos de enfermedades inflamatorias intestinales). Además, si nuestra microbiota se encuentra alterada, nuestra salud metabólica también empeorará.
Es decir, la alteración del equilibrio de nuestra microbiota se traduce en un empeoramiento de nuestra salud y por lo tanto, en un mayor riesgo de sufrir enfermedades crónicas. De hecho, la disbiosis de la microbiota intestinal se encuentra asociada a diversos desórdenes, entre los que se encuentra la diabetes, la obesidad, diferentes tipos de cáncer (especialmente el colorrectal), alergias, síndrome metabólico, así como la enfermedad inflamatoria intestinal. Se ha comprobado que los individuos que padecen estas enfermedades suelen presentar disbiosis intestinal, bien sea por una excesiva presencia de bacterias patógenas, por una falta de microorganismos beneficiosos o por la falta de diversidad.
En realidad, no sabemos con claridad si estas enfermedades en sí son las causantes de la disbiosis intestinal o si la aparición de la disbiosis es anterior y es la que aumenta el riesgo de la enfermedad. Aunque no sepamos con total certeza cuál es la causa y cuál es el resultado, lo que sí podemos afirmar es que, en ambos casos, nuestros hábitos juegan un papel fundamental tanto en la prevención como en el transcurso del tratamiento, ya que existe una amplia evidencia científica demostrando cómo la alimentación y los hábitos de vida resultan esenciales para que exista un correcto equilibrio en nuestra microbiota.
Principales causas de la disbiosis intestinal
Antibióticos
Los antibióticos, cuando son necesarios, salvan vidas. Pero hay que hacer un especial énfasis en que hay que tomarlos cuando verdaderamente haga falta. Entre los principales problemas que ocasiona el mal uso de los antibióticos no sólo se encuentra la alteración de la microbiota intestinal, sino también la resistencia que nuestras bacterias generan hacia ellos. La resistencia a los antibióticos significa que las bacterias patógenas mutan en respuesta al uso de estos fármacos y esto ocasiona que las infecciones resulten mucho más letales, ya que su tratamiento se dificulta en gran medida porque los antibióticos dejan de ser efectivos.
El aumento de resistencia a los antibióticos también se está debiendo a su uso en la ganadería. Actualmente, la carne que generalmente se toma viene de animales a los que se le han administrado antibióticos, que incluso se emplean como “medida preventiva” para que los animales no sufran infecciones. Este uso de antibióticos, muchas veces indebido, está siendo una de las causas subyacentes del significativo aumento de resistencia a los antibióticos. Según la OMS, se trata de un problema muy serio que no para de aumentar. Por ese motivo, resulta esencial ser muy cauteloso acerca del consumo de antibióticos: en el caso de que resulten necesarios, deben siempre tomarse bajo el seguimiento e indicaciones del médico.
Sin embargo, debemos ser conscientes de que buena parte de las infecciones se pueden prevenir, y no solo mediante una correcta higiene, sino también con una alimentación saludable y unos buenos hábitos, que mantengan sana y fuerte a nuestra microbiota intestinal. Esto repercutirá positivamente sobre nuestra respuesta inmunológica y por tanto, tendremos menor riesgo de enfermar.
Alimentación alta en proteína de origen animal
Se ha demostrado que la elevada ingesta de proteína animal, especialmente la que proviene de carne roja y carne procesada, puede deteriorar el estado de nuestra microbiota y aumentar el riesgo de cáncer colorrectal. Seguir una dieta rica en carne roja y en carne procesada ha demostrado ejercer una acción inflamatoria y carcinogénica, que promueve la disfunción de nuestra barrera intestinal, el daño en el ADN y además, tiene un efecto genotóxico.
Desgraciadamente, el consumo actual de carne procesada es en muchos casos exagerado, ya que es común ver cómo se toma embutido prácticamente a diario, en forma de bocadillos o en las cenas. En cuanto a la carne, su consumo, en términos generales, también es bastante elevado. Esto, tal y como nos muestran los estudios científicos realizados al respecto, no sólo deteriora la salud de nuestra microbiota y promueve su alteración, sino que también puede aumentar el riesgo de cáncer, se ha visto asociado a un mayor riesgo de enfermedad cardiovascular y también de diabetes tipo 2.
Baja ingesta de verduras y frutas
Las frutas y verduras deben constituir el elemento más abundante de nuestra alimentación. En cada comida del día, las frutas y las verduras deben ser las protagonistas. Son la mejor fuente de compuestos bioactivos con acción antioxidante, como los flavonoides, entre los que se encuentran las catequinas, la quercetina, las antocianinas y la rutina, entre otros; además, también son una excelente fuente de carotenoides (betacaroteno, luteína, licopeno…) y otros polifenoles como el ácido elágico. Estos compuestos dotan a las frutas y verduras de una importante acción antiinflamatoria y antioxidante, lo cual estimula la producción de los tan importantes ácidos grasos de cadena corta por parte de nuestras bacterias intestinales.
Además, las verduras y las frutas abundan en fibras fermentables, con acción prebiótica, como la pectina (se encuentra en la mayoría de frutas, siendo la manzana la que de las que más contiene), el almidón resistente (abunda en el plátano verde, en los boniatos y las patatas), los betaglucanos (las verduras que presentan un mayor contenido son las setas) y los fructanos (alcachofas, cebollas, puerros, espárragos). Estas fibras sirven de alimento para nuestras bacterias beneficiosas intestinales, estimulando su producción de ácidos grasos de cadena corta como el butirato.
El bajo consumo de frutas y verduras no resultará positivo para nuestra microbiota intestinal, ya que no obtendremos los beneficios mencionados. Además, si uno consume pocas verduras y hortalizas, significará que hay otros alimentos que están ocupando la base de la dieta, como los productos ultraprocesados (galletas, postres lácteos, cereales refinados, bollos, pizzas, salsas, etc.), la carne roja y la procesada, los cuales deterioran la salud de la microbiota y pueden a la larga provocar su alteración.
Baja ingesta de fibra
Las mejores fuentes de fibra son los alimentos de origen vegetal sin procesar (o mínimamente procesados): las verduras y hortalizas (brócoli, calabaza, tomates, alcachofas, espinacas, etc.), las frutas enteras (no en zumo), las legumbres (lentejas, garbanzos, alubias, guisantes), los granos integrales (copos de avena integral, el trigo sarraceno, quinoa y el arroz integral son los más recomendables), los frutos secos naturales (sin sal, ni fritos ni tostados) y también las semillas oleaginosas como las de lino y las de calabaza.
La fibra juega un papel fundamental en nuestra microbiota, en concreto la fibra fermentable, ya que ejerce una acción prebiótica. El alto consumo de fibra de forma prolongada en el tiempo está asociado con un menor riesgo de cáncer colorrectal y también de cáncer de mama. La fibra presente en los alimentos mencionados anteriormente es fermentada por nuestras bacterias beneficiosas intestinales y entre los productos resultantes de dicha fermentación, se encuentran los ácidos grasos de cadena corta. En particular, el butirato ha demostrado que ayuda a mantener la buena salud de los colonocitos, intensifica el proceso de apoptosis y actúa inhibiendo la proliferación de las células cancerígenas. Por si esto fuera poco, la fibra ayuda a eliminar los posibles carcinógenos presentes en nuestro intestino, ya que aumenta el tamaño de las heces y mejora la motilidad intestinal.
Una ingesta insuficiente de fibra se traducirá en un empeoramiento del estado de nuestra microbiota, ya que no estaremos obteniendo la protección que nos proporciona la fibra procedente de alimentos enteros de origen vegetal frente al cáncer, la diabetes, la enfermedad cardiovascular y la obesidad.
Obesidad y sobrepeso
Se ha demostrado que las personas con un exceso de peso presentan una microbiota alterada, por lo que mantener un peso saludable resulta también clave para evitar la disbiosis intestinal. La disbiosis intestinal también puede provocar un desequilibrio de la homeostasis energética, lo cual puede conducir a la ganancia de peso y la obesidad. Podríamos entonces decir que el estado de nuestra microbiota influye en gran medida sobre nuestra salud metabólica. Y mantenerla en buen estado, sin romper su equilibrio, nos ayuda a mantener un peso saludable.
En resumen, la disbiosis intestinal se suele asociar a síntomas digestivos, pero hay muchos más:
– Dolor abdominal
– Diarrea o estreñimiento
– Aumento de gases
– Inflamación e hinchazón abdominal
– Sensibilidad alimentaria e intolerancias
– Dolores de cabeza
– Dolores musculares y articulares
– Candidiasis
– Enfermedades autoinmunes como Diabetes mellitus tipo I, Enfermedad de Crohn, Hashimoto, psoriasis…
– Problemas cutáneos como eczema, acné, dermatitis…
– Infecciones de repetición: cistitis, otitis, amigdalitis, faringitis…
– Problemas hormonales…
– Estrés, ansiedad
– Migrañas…
Si tienes otras dudas puedes revisar nuestra sección de Preguntas Frecuentes, o comenzar ahora con tu tratamiento agendando una hora con nosotros

